腫瘤細胞的保護性自噬及其DNA損傷修複是腫瘤治療耐受的重要原因,放射醫學與輻射防護國家重點實驗室、醫學部放射醫學與防護學院分子影像與核醫學研究中心發現Au@Cu2-xSe納米顆粒抑制腦膠質瘤細胞保護性自噬和DNA損傷修複增強放療療效的新機制。相關成果以“Inhibiting autophagy flux and DNA repair of tumor cells to boost radiotherapy of orthotopic glioblastoma”為題發表在Biomaterials雜志上(Biomaterials 280 (2022) 121287)。論文鍊接:https://doi.org/10.1016/j.biomaterials.2021.121287。
放療是腦膠質瘤治療的常用手段。然而,放療使腫瘤細胞産生保護性自噬,降低對其DNA的持續性損傷,導緻腦膠質瘤産生很強的放療耐受,克服放療耐受對提高其放療效果具有重要意義。在前期工作中,分子影像與核醫學研究中心團隊構建了“大成若缺、富含空位”的Cu2-xSe超小納米顆粒。這種納米顆粒具有豐富的内在新穎性質,如光熱、光動力、化學動力、放射增敏等,不僅可用于腫瘤的成像和治療(Adv. Mater. 2016, 28, 8927–8936;Nano Lett, 2018, 18, 4985-4992;Nanoscale, 2019, 11, 7600–7608; ACS Appl. Mater. Interfaces 2019, 11, 16367−16379;Adv. Funct. Mater. 2020, 30, 1906128;Adv. Funct. Mater. 2021, 202108971);而且還可用于帕金森疾病的治療(J. Am. Chem. Soc. 2020, 142, 21730−21742)。為了增強Cu2-xSe納米顆粒的成像和治療效果,研究團隊還對其進行功能化,顯著提高其診療效果(ACS Nano, 2017, 11, 5633-5645; ACS Nano, 2019, 13,1342-1353; ACS Appl. Mater. Interfaces 2020, 12, 4231−4240)。
在上述研究基礎上,本研究構建了具有核殼結構的Au@Cu2-xSe納米顆粒,通過抑制腫瘤細胞保護性自噬,降低放療引起的DNA損傷修複,從而提高腦膠質瘤的放療效果。研究發現Au@Cu2-xSe 納米顆粒一方面通過改變腫瘤細胞溶酶體的酸堿度,有效抑制自噬流,促使其SQSTM1/p62蛋白水平上調;另一方面,它們促進DNA損傷修複的關鍵蛋白Rad51泛素化,使其被蛋白酶體系統降解,阻礙放療過程中的DNA損傷修複。納米顆粒通過同時抑制放療引發的保護性自噬及DNA損傷修複,明顯抑制原位腦膠質瘤生長,顯著提高了放療療效。該研究為合理設計用于抑制腫瘤細胞保護性自噬和DNA損傷修複增強療效的納米顆粒提供了新思路。
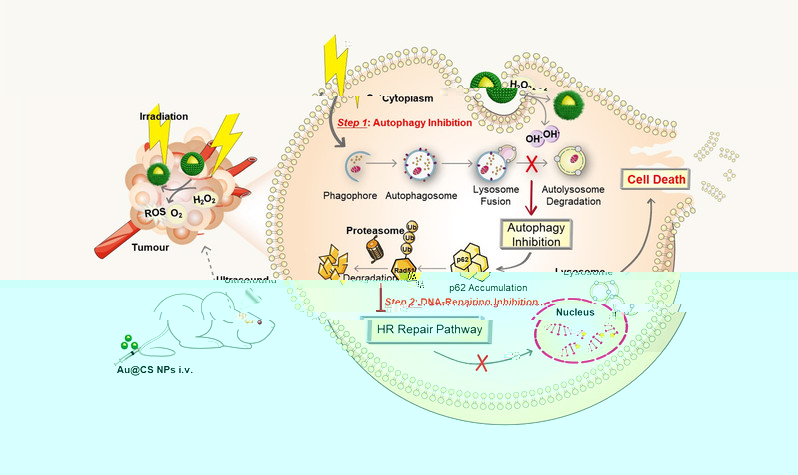 圖1. Au@Cu2-xSe納米顆粒抑制腫瘤細胞自噬流、阻礙DNA損傷修複及提高放療敏感性的示意圖
圖1. Au@Cu2-xSe納米顆粒抑制腫瘤細胞自噬流、阻礙DNA損傷修複及提高放療敏感性的示意圖
放射醫學與輻射防護國家重點實驗室、醫學部放射醫學與防護學院為論文第一單位,論文第一作者為beat365正版放射醫學與防護學院的碩士生許琦,張浩博士和李桢教授為該文章的通訊作者。該研究得到了國家自然科學基金(81971671),國家重點研發計劃(2018YFA0208800),江蘇省重點研發計劃(BE2019660)等項目的支持。